全球首创植物源重组人血清白蛋白获批上市
7月18日,国家药品监督管理局官网显示,禾元生物申报的植物源重组人血清白蛋白(HY1001)获批上市,用于肝硬化低白蛋白血症的治疗。此前已于2024年8月被CDE纳入优先审评。
目前,临床使用的人血清白蛋白药物均来自人类血浆的分离提取,存在资源短缺和病原体传播的风险。据公开资料显示,2020年国内人血清白蛋白治疗药物市场规模已高达258亿元人民币,且进口依赖严重,进口产品长期占据60% 以上的市场,人血清白蛋白仍存在较大供需缺口。
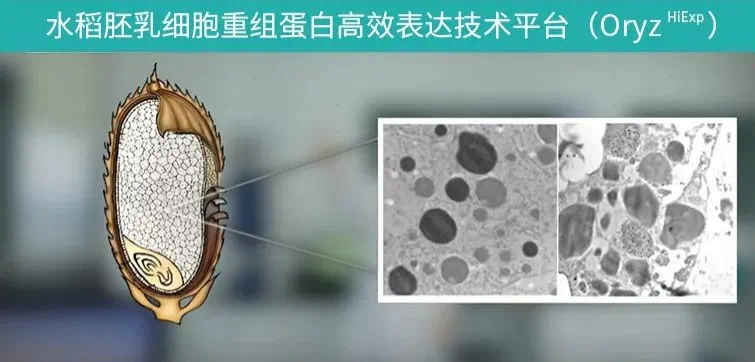
HY1001是禾元生物首个研发的重磅产品,利用水稻胚乳细胞表达,经提取、纯化的重组人血清白蛋白产品,成功解决了重组人血清白蛋白的纯度、规模化和成本问题,更实现了从源头上杜绝病毒传播的风险,确保了血液制品的安全性。此次 HY1001的获批,标志着禾元生物在全球首创的植物重组蛋白质药物领域取得了显著进展,有望解决我国人血清白蛋白长期依赖进口的局面。
2025年6月,禾元生物一项关于 HY1001 的临床研究在《Gut》上发表。这是一项多中心、随机双盲、阳性对照(基立福的Albutein)的Ⅱ期研究,按照中国CDE和美国FDA共同认可的临床方案进行,对220例肝硬化腹水患者进行静脉注射给药,每日剂量高达20g,连续注射最长14天。
研究结果显示,HY1001 能显著提升白蛋白水平,14天内血清白蛋白浓度达到35g/L的受试者比例非劣效于阳性对照组,且升高胶体渗透压、达标中位时间、血清白蛋白变化值、体重腹围改善等与阳性对照无统计学差异;未发生药物相关严重不良反应,安全性良好;没有产生有临床意义的抗药抗体和抗HCP抗体,宿主蛋白免疫原性低。
2024年11月,禾元生物宣布HY1001在肝硬化低白蛋白血症患者中的 Ⅲ期头对头血浆来源人血清白蛋白的临床(CTR20230244)达到研究终点。数据显示,HY1001的疗效不劣于对照人血清白蛋白,且安全性良好。
2024年9月,贝达药业和禾元生物就 HY1001签署药品区域经销协议。贝达药业获得在约定区域内独家经销HY1001的权利。
据记者了解,除了HY1001,禾元生物还有5款产品进入临床阶段(含批准临床)。
*重组人乳铁蛋白溶菌酶-HY1002是一款针对儿童轮状病毒引起腹泻的一款广谱抗病毒和细菌感染的口服复合制剂,主要成分来自母乳中的主要成分,具有相容好和安全性高的特点,对婴幼儿更加安全。目前已完成国内Ⅱ期临床试验。
*HY1003是一款植物源重组α-1抗胰蛋白酶,也是禾元生物获得的首个FDA孤儿药认定品种。按照市场容量的30%计,预计该药将拥有超 30亿美元的美国市场和约 1000亿美元的全球市场。目前已完成在美国开展的I期临床试验。
*植物源重组瑞替普酶-HY1004是禾元生物研发的第三代溶栓药物,可以使纤维蛋白溶解酶原激活为有活性的纤溶蛋白溶解酶,以降解血栓中的纤维蛋白,发挥溶栓作用。该药适用于成人由冠状动脉梗塞引起的急性心肌梗塞的溶栓疗法,能够改善心肌梗塞后的心室功能。
*口服重组人糜蛋白酶冻干粉-HY1005是从基因工程水稻稻谷中提取和纯化重组人糜蛋白酶原,通过激活获得具有生物活性的重组人糜蛋白酶,适应症为用于胃镜检查时溶解去除胃内黏液。
*重组人糜蛋白酶-HY1005 是国际上首个重组人糜蛋白酶药物,与天然人糜蛋白酶具有相同的生物活性,临床默示许可适应症为胸膜炎。目前该药已完成针对胸膜炎适应症的I期临床研究单次给药阶段的全部受试者入组。
(长江云新闻记者 王丹 通讯员 陈登梅)







 社会保障
社会保障 交通出行
交通出行 公积金
公积金 公安服务
公安服务 职业资格
职业资格 医疗健康
医疗健康 市场监管
市场监管 法律服务
法律服务
 融媒体平台建设服务
融媒体平台建设服务 长江云 • 新时代文明实践平台
长江云 • 新时代文明实践平台

 大数据舆情中心
大数据舆情中心